DNK je nukleinska kislina z vplivom na različne (pato)fiziološke funkcije. Na raznolikost njenega delovanja pomembno vplivajo različne prostorske strukture, v katere se zvija, vpogled v te strukture pa omogoča pripravo njenega celovitega opisa, ki ga potrebujemo za razvoj novih načinov zdravljenja. Prav ta vpogled v strukture nam omogoča metoda jedrske oziroma nuklearne magnetne resonance (NMR). NMR je fizikalni pojav, ki opisuje interakcijo magnetnih momentov atomskih jeder z elektromagnetnim poljem s frekvenco, ki je enaka frekvenci atomskih jeder. Na Kemijskem inštitutu v Ljubljani deluje mednarodno uveljavljen NMR center, v okviru katerega potekajo strukturne študije biomakromolekul, vključno s strukturnimi študijami fragmentov DNK. Kot smo že omenili, se DNK lahko zvije v različne prostorske strukture, med katerimi so še posebno zanimivi štirivijačni G‑kvadrupleksi, ki so vključeni v pereče nevrodegenerativne motnje, njihove raznolike funkcije pa imajo potencialno zaščitne ali škodljive učinke v razvoju nevroloških bolezni. Čeprav so študije njihovega delovanja funkcij in vivo še v začetni fazi, rezultati že kažejo, kolikšen je njihov biološki pomen. Boljše razumevanje prostorske strukture G‑kvadrupleksov je pomembno za razkritje njihovih morebitnih vlog v patogenezi bolezni, kot je nevrodegeneracija, ter za oblikovanje novih načinov diagnosticiranja in zdravljenja. Nedavno odkriti kvadrupleksi AGCGA – nova štirivijačna strukturna družina, ki jo je odkrila naša skupina in o kateri bo še tekla beseda – se nahajajo v regulatorni regiji gena PLEKHG3, ki prispeva k tveganju za avtizem in ima zato velik biološki pomen. Ponavljajoča se zaporedja AGCGA se nahajajo v regulatornih regijah vsaj 38 različnih človeških genov, povezanih z razvojem možganov in nevrološkimi motnjami, nenormalnimi hrustančnimi in kostnimi formacijami, rakom in regulacijo osnovnih celičnih procesov. Poleg preučitve strukturnih zdravljenja lastnosti DNK ima pomembno vlogo pri razvoju zdravljenja tudi oblikovanje ustreznega dostavnega sistema. Ena izmed možnosti za dostavo kompleksnih struktur DNK so zunajcelični vezikli – učinkovit in stabilen dostavni sistem, tudi za G‑kvadruplekse. A pojdimo po vrsti.
Ključne strukturne značilnosti dvovijačne DNK
DNK je nerazvejan polimer, katerega osnovna enota je nukleotid. Nukleotid je sestavljen iz sladkorja (2'‑deoksiriboza), dušikove spojine (štiri osnovne baze se imenujejo adenin, citozin, gvanin in timin) in fosfatne skupine. Ker so baze štiri, imamo torej štiri različne nukleotide (A, C, G in T), katerih zaporedje kot nekakšna abeceda zapisuje informacijo.
- Verigi iz različnih nukleotidov, ki se ovijata okoli skupne osi, tvorita desnosučno vijačnico. Pri tem se dušikove baze nahajajo na notranji strani vijačnice in so medsebojno povezane v bazne pare. Adenin je vedno v paru s timinom, citozin pa z gvaninom (Watson‑Crickovo pravilo baznih parov).
- Verigi sta antiparalelni, kar pomeni, da tečejo povezave med sosednjimi deoksiribozami (preko fosfatnih skupin) v nasprotnih si smereh.
- Vzdolž natančno urejene vijačnice potekata mali in veliki žleb, ki sta značilni topografski posebnosti dvojne vijačnice DNK.
- V vodnem okolju se polarno in nabito kovalentno ogrodje iz izmenjujočih se deoksiriboz in fosfatnih skupin nahaja na zunanji strani vijačnice, zato tvori interakcijo z vodo. Dušikove baze, ki so v notranjosti vijačnice, pa so hidrofobne in se vodi raje izognejo. Pomemben element stabilnosti prostorske strukture je tudi medsebojno delovanje s pozitivnimi kovinskimi kationi iz okolice.
- Dvojna vijačnica je zaradi različnih vrst vezi oziroma interakcij zelo stabilna. Najmočnejše so vodikove vezi med pari komplementarnih baz na nasprotnih si verigah, ki skrbijo, da sta verigi trdno povezani. Za razumevanje stabilnosti moramo upoštevati tudi medmolekularne sile in hidrofobne interakcije med naloženimi bazami – te so šibkejše, a dajejo dodatno stabilnost.
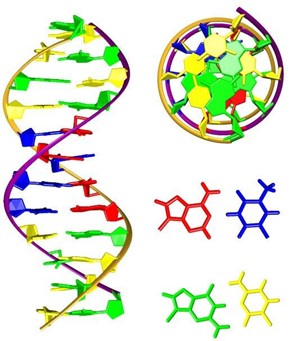
Slika 1: Dvojna vijačnica DNK. Prikazana sta pogleda od strani in od zgoraj ter bazna para AT (adenin in timin) in GC (gvanin in citozin).
G‑kvadrupleks – ena od pestrih prostorskih oblik DNK
V splošnem še vedno velja, da je glavna vloga DNK shranjevanje bioloških informacij, ni pa edina. Konci DNK se imenujejo telomere – to so skrajni deli linearnih kromosomov – kjer so zaporedja ponavljajoča se in vsebujejo nesorazmerno veliko gvaninskih (G) nukleotidov, precej manj pa ostalih treh (označenih s črkami A, T in C). Zaradi posebnih značilnosti gvanina lahko takšna zaporedja v prostoru namesto dvojne vijačnice zavzamejo drugačno obliko, ki jo imenujemo G‑kvadrupleks, saj gre za štirivijačno strukturo. V tej strukturi gvaninske baze niso povezane v bazne pare, temveč v kvartete, ki jim kovinski kationi v sredini nudijo dodatno stabilizacijo. Že prve študije ob koncu 20. stoletja so nakazovale, da takšen G‑kvadrupleks ščiti konec DNK in preprečuje, da bi ga encimi, ki so vpleteni v popravilo poškodovane DNK, obravnavali kot poškodbo. Konce DNK si torej lahko predstavljamo kot zaščito ladijskih vrvi ali jeklenic, ki so na koncih zlepljene, da se ne razpletejo.
Vidimo torej, da se DNK lahko zvije v različne prostorske strukture, ne le v šolsko dvojno vijačnico, kar je odvisno od zaporedja nukleotidov (»črk«) v posameznem predelu DNK. To omogoča, da lahko molekula izvaja različne biološke funkcije, vse od prenosa genskih informacij do katalize in regulacije. Dvovijačna DNK, ki kodira človeški genom, obstaja v celicah skupaj z omenjenimi G‑kvadrupleksnimi strukturami, za katere je dokazano, da so vpete v pomembne biološke funkcije. Bioinformatske analize in sekvenciranje človeškega genoma so pokazali, da je število zaporedij, ki se lahko zvijejo v G‑kvadrupleksne strukture, večje od 700.000.
V človeškem genomu so območja, ki so sposobna zvitja v G‑kvadrupleks, pogosteje prisotna na mestu, kjer se začne genska informacija posameznega gena z DNK brati in prepisovati (pravimo, da gre za začetek transkripcije, kar se zgodi v 5'‑neprevedeni regiji in na koncu prvega introna). Tvorba G‑kvadrupleksov je pomembno povezana z onkogeni (geni, katerih aktivacija lahko povzroči raka), supresorji tumorjev (geni, ki zavirajo nastanek tumorjev) in spremembami somatskih kopij, udeleženih pri razvoju raka. Vse več eksperimentalnih podatkov podpira hipotezo, da so G‑kvadrupleksi, ki se tvorijo v zaporedjih na mestu tik pred začetkom prepisa (promotorska zaporedja), vključeni v uravnavanje ekspresije, torej tega, kdaj in kako se posamezni geni dejansko izrazijo. Opazovanje tvorbe štirivijačnih struktur v promotorjih znotraj živih celic je pokazalo, da regulacijska vloga pri transkripciji ni vezana samo na prisotnost z gvanini bogatega zaporedja, ampak je pomembna predvsem strukturna sprememba iz šolske dvojne vijačnice v kvadrupleksno strukturo. Tudi štirivijačnih struktur je več vrst – s citozini bogate regije DNK se zvijajo še drugače, in sicer v i‑motive: osnovni strukturni element predstavljata citozinski bazi, ki ju povezujejo tri vodikove vezi (Slika 2).
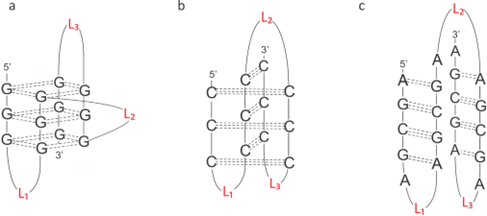
Slika 2: Shematska predstavitev štirivijačnih struktur DNK: a) G‑kvadrupleks, b) i‑motiv, c) AGCGA‑kvadrupleks. Oznake L1, L2 in L3 predstavljajo zanke z različnimi dolžinami in sestavo nukleotidov. Zanke povezujejo pramene, ti pa tvorijo jedro struktur. S črtkanimi črtami so označene vodikove vezi.
Odkritje nove štirivijačne strukturne družine
Nedavno je naša skupina odkrila novo štirivijačno strukturno družino, ki smo jo poimenovali AGCGA‑kvadrupleksi. Pokazali smo, da zaporedje d(GGGAGCGAGGGAGCG), ki smo ga poimenovali VK1 in ga najdemo v regulatornem območju gena PLEKHG3 v 14. človeškem kromosomu, tvori nov tip štirivijačne strukture. Poudariti velja, da zaporedje VK1 izpolnjuje kriterije za tvorbo G‑kvadrupleksa, ki pa se ne tvori. Druga zanimiva značilnost VK1 in sorodnih zaporedij je, da se zvijejo v prisotnosti litijevih kationov. Nasprotno pa je že nekaj časa znano, da zvijanje z gvanini bogatih oligonukleotidov v dobro definirano G‑kvadrupleksno strukturo zahteva prisotnost kalija (K+), natrija (Na+) ali drugih kationov (ki so lahko tudi večvalentni). Vloga kationov pri tvorbi raznolikih prostorskih struktur DNK še ni v celoti pojasnjena in je predmet številnih študij. Prostorska struktura DNK, v katero se zvije zaporedje VK1, se zelo razlikuje od pričakovane strukture G‑kvadrupleksa, kar je presenetljivo, saj primarno zaporedje vsebuje dva segmenta GGG. Kljub temu je struktura stabilna, saj za stabilizacijo poskrbijo interakcije med drugimi deli.
Strukturne študije z NMR-spektroskopijo so pomembne z več vidikov
G‑ in AGCGA‑kvadrupleksi so s strukturnega vidika izredno zanimivi, zlasti zaradi svoje velike raznolikosti (Slika 2). Eden večjih izzivov, ki še ni zadovoljivo rešen, je napovedovanje oblike zvitja zgolj na osnovi zaporedja nukleotidov. V zadnjih letih smo s pomočjo NMR‑spektroskopije v raztopini preučevali strukturne značilnosti in dinamične lastnosti kationov, vezanih znotraj G‑kvadrupleksnih struktur, ki jih tvorijo zaporedja, bogata z gvanini, na telomernih koncih in v promotorjih različnih genov.
Nepopolno poznavanje strukturnih značilnosti kvadrupleksov je eden od razlogov, da se osredotočamo prav na ta biološko pomembna zaporedja. Boljše razumevanje bioloških funkcij nukleinskih kislin zahteva informacijo tako o strukturi molekule kot tudi o njeni dinamiki. Uporaba večjedrnih NMR‑eksperimentov z visoko ločljivostjo ponuja vpogled v ravnovesje (ki ga določa termodinamika) in zvijanje molekul (kjer je ključnega pomena hitrost zvijanja v posamezne strukture). Končna cilja raziskav sta poznavanje molekulske 3D‑strukture v raztopini z atomsko ločljivostjo ter celovit opis s fizikalno‑kemijskega vidika. Takšno znanje je osnova za načrtovanje novih organskih molekul, ki bi lahko pripomogle v boju proti različnim oblikam raka in številnim virusnim obolenjem.
Poglobljeno razumevanje procesov, ki vodijo spremembo DNK iz dvovijačne strukture v štirivijačno (kot sta G‑ ali AGCGA‑kvadrupleks), je nujno za razvoj novih načinov zdravljenja. Štirivijačne strukture DNK ponujajo alternativen pristop pri usmerjenem delovanju na nukleinsko kislino, ki vključuje prepoznavanje struktur višjega reda, kar je osnova za močno vezavo ligandov (molekul z majhno molekulsko maso) in njihovo sistematično iskanje oziroma kemijsko načrtovanje. Pri iskanju ligandov, ki bi bili selektivni za G‑kvadruplekse ali druge prostorske strukture DNK, so študije pripeljale do različnih heterocikličnih sistemov. Velik del načrtovanja še vedno upošteva načelo, da naj bi se skelet molekule liganda dobro prilegal na (zunanji) G‑kvartet. Naša skupina je nedavno odkrila in v mednarodni periodiki opisala prostorsko strukturo kompleksa med G‑kvadrupleksom, ki ga tvori človeško telomerno zaporedje, in ligandom (PhenDC3). Posebna zanimivost te strukture kompleksa je dejstvo, da se je ligand ugnezdil (interkaliral) med dve G‑kvartetni ravnini, kar je prvi opisani primer v svetu in kot tak odpira številne nove premisleke. Takšne strukturne podatke lahko uporabimo pri načrtovanju novih interkalirajočih ligandov.
Kot smo že uvodoma omenili, so zunajcelični vezikli ena izmed možnosti za dostavo kompleksnih struktur DNK – postali bi lahko stabilen dostavni sistem tudi za G‑kvadruplekse.
Zunajcelični vezikli – ena izmed možnosti za vezavo molekul v G‑kvadrupleksno strukturo
Nukleinske kisline so občutljive molekule, zato zahtevajo v primeru vnosa v človeški organizem ustrezen dostavni sistem. Ena izmed možnosti za aplikacijo izbrane nukleinske kisline (po potrditvi njene strukture in dokazani učinkovitosti) je vključitev v zunajcelične vezikle, ki so eden izmed novejših načinov dostave molekul. Zunajcelični vezikli so lipidni dvoslojni delci nanometrske velikosti, ki jih sproščajo različni celični organizmi. Izhajajo iz naravnih organizmov in imajo zaradi znane biološke vloge ter svoje sestave več prednosti pred podobnimi sinteznimi dostavnimi sistemi, kot so liposomi in polimerni sintezni nanodelci. Za naravne zunajcelične vezikle sta namreč značilni nizka imunogenost in nizka toksičnost, kar je pomembno za čim boljši učinek dostavljene biomolekule. Dvoslojna lipidna površina dobro ščiti občutljivo biomolekulo pred razgradnjo zaradi nizkega pH ali encimov.
Privzem zunajceličnih veziklov v človeške celice je pogosto zelo učinkovit, saj lipidni dvosloj omogoča zlitje z membranami človeških celic, k čemur pripomorejo tudi številni membranski proteini v njem. Dodatno lahko površino vezikla spremenimo z različnimi reagenti. Z biomodificiranjem površine vezikla lahko vplivamo na specifičnost dostave biomolekule, in sicer v smislu merjenja na točno določeno tkivo oziroma celice znotraj človeškega organizma. Eden izmed možnih načinov usmerjanja vezikla je, da na njegovo površino pripnemo protitelo, ki vezikel usmeri na mesto delovanja.
V literaturi je objavljenih več primerov uspešne vgradnje nukleinske kisline v vezikel in možnostih uporabe v terapiji. Vezikle kot dostavne sisteme za nukleinske kisline, predvsem molekule RNK, so v raziskavah uspešno preizkusili za zdravljenje različnih rakavih in genskih bolezni, tudi nevrodegenerativnih obolenj, saj vezikli zaradi svoje majhnosti in lipidnega dvosloja omogočajo prehajanje krvno-možganske pregrade. Poleg RNK se v vezikle lahko vključi tudi DNK. Čeprav je v literaturi takih primerov manj, so že opisani posamezni primeri uspešne vključitve DNK v vezikel, na primer pri genskih škarjah CRISPR/Cas9 za gensko modificiranje, ki omogoča različne možnosti uporabe v biotehnološke in biomedicinske namene. V nedavno objavljeni raziskavi pa so v vezikle, pridobljene iz matičnih celic, vključili celo G‑kvadrupleksne strukture in jih uporabili pri zmanjšanju imunosupresivne funkcije imunskih celic s ciljem zdravljenja malignih tumorjev. Raziskava podpira velik potencial uporabe zunajceličnih veziklov kot načinov za dostavo terapevtskih nukleinskih kislin na ciljano mesto aplikacije.

Slika 3: Shematska predstavitev vključitve DNK v zunajcelični vezikel, modificiranja površine vezikla z uporabo tarčnih protiteles in privzema tarčno usmerjenega zunajceličnega vezikla v tumorsko celico.
Če povzamemo: da bi lahko kompleksne oblike DNK vključili v dostavni sistem, mora ta omogočati ohranitev lastnosti in aktivnosti DNK. Eden izmed načinov je vključitev v zunajcelične vezikle, ki poleg učinkovite vgraditve omogočajo tudi zaščito občutljive vsebine. Modificiranje površine veziklov odpira tudi možnost učinkovite in tarčno usmerjene dostave terapevtske DNK na točno določeno prizadeto mesto v človeškem organizmu. Natančnost strukturnih raziskav na področju razumevanja kompleksnosti DNK, njene dinamike v bližnjem okolju in njene vključitve v učinkovit dostavni sistem tako predstavljajo ključne korake pri oblikovanju načinov zdravljenja (različnih oblik raka, nevrodegenerativnih bolezni in virusnih obolenj).