Sir Isaac Newton je alkimiji namenil več časa in besed kot matematiki in fiziki skupaj. Skozi stoletja se je alkimistov prijel slab sloves, bili so tarča posmeha in pogosto označeni za nore pristaše ezoterike. Angleška spiritualistična pisateljica 19. stoletja Mary Anne Atwood je celo zapisala: »Nobena sodobna umetnost ali kemija, ne glede na vse svoje neznanke, nima nobene povezave z alkimijo.« Pa so si alkimisti res zaslužili to, kar se je o njih govorilo?
Alkimisti so bili predani temu, da bi iz običajnih kovin proizvedli žlahtne kovine in elemente, ki bi delovali kot eliksir nesmrtnosti in modrosti ter tako ozdravili vse bolezni. Eden najbolj želenih produktov alkimije je bilo zlato, najpogostejši začetni kovini za pretvorbo pa sta bili svinec in živo srebro. Končnega cilja jim nikoli ni uspelo doseči, kljub vsemu pa je alkimija uveljavila številne laboratorijske tehnike, teorije in izraze, ki se še vedno uporabljajo v moderni kemiji.
Povezava alkimije in jedrske fizike tiči v atomskem jedru, kjer najdemo protone in nevtrone. Število protonov določa identiteto kemijskega elementa; tako je na primer element z enim protonom vodik, z dvema helij, s tremi bor ipd. Različno število nevtronov pri enakem številu protonov pa daje elementu različne izotope. Jedrske reakcije zajemajo vse reakcije, ki vključujejo atomsko jedro in spremenijo njegovo sestavo. Za te reakcije je značilno, da jih spremlja radioaktivni razpad, ki je posledica nastanka presežka energije ali nestabilnih izotopov. Tri glavne vrste radioaktivnega razpada so alfa, beta in gama. Pri razpadu alfa pride do izsevanja helijevega jedra (dva protona in dva nevtrona), pri razpadu beta do izsevanja elektrona ali pozitrona, pri razpadu gama pa do izsevanja žarkov gama (žarki z visoko energijo in kratko valovno dolžino). Če jedrska reakcija in radioaktivni razpad privedeta do pretvorbe iz enega kemijskega elementa v drugega, se ta pretvorba imenuje transmutacija.
Vendar pa so bili alkimisti do neke mere blizu resnice – živo srebro (Hg) danes znamo spremeniti v zlato (Au), pomagamo pa si z jedrsko fiziko. Pretvorba se začne z majhno količino raztopine živega srebra, ki jo zatalimo v stekleno ampulo. Ampulo z živim srebrom moramo nato obstreljevati (obsevati) s termalnimi oziroma počasnimi nevtroni, ki pogosteje trčijo s tarčo kot hitri nevtroni. Potrebujemo torej vir nevtronov, za kar lahko uporabimo različne pospeševalnike, zlasti pa je za to primeren jedrski reaktor. Ko se zgodi uspešen trk nevtrona z atomom živega srebra, postane jedro slednjega zaradi visokega presežka energije nestabilno. Ta energija se mora nekako sprostiti, kar se zgodi preko jedrske reakcije in radioaktivnega sevanja. Če se trk zgodi med nevtronom in izotopom živega srebra 196Hg, se del živega srebra pretvori v nestabilni izotop 197Hg, ki pa zaradi svojega nestabilnega vzbujenega stanja radioaktivno razpade v izotop zlata 197Au. Ta izotop zlata je stabilen in ostane v raztopini. Tako lahko s pomočjo transmutacije živo srebro pretvorimo v zlato. Jedrska fizika izkorišča transmutacijo tudi za pretvorbo mnogih drugih elementov. Seveda transmutacije v tej obliki alkimisti niso poznali (niti sodobnega koncepta kemijskih elementov), so pa izbrali ustrezna reaktant in produkt – živo srebro in zlato. Izbira živega srebra je bila vizionarska tudi zato, ker sta živo srebro in zlato soseda v periodnem sistemu elementov, ki pa ga alkimisti takrat še niso poznali.
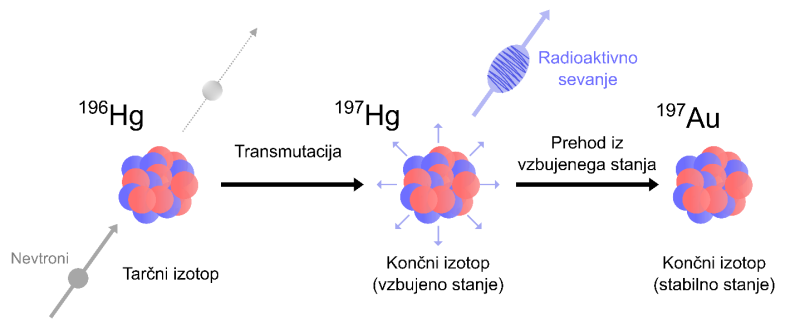
Proces transmutacije izotopa živega srebra do zlata preko obsevanja z nevtroni (prirejeno po Chouhan idr. 2023)
Na Odseku za znanosti o okolju (O2) Instituta "Jožef Stefan" sodelujemo z Reaktorskim infrastrukturnim centrom (RIC) pri obsevanju živega srebra z nevtroni v raziskovalnem reaktorju TRIGA. Osnovni namen ni pretvorba živega srebra v zlato, temveč uporaba vmesnega produkta transmutacije (197Hg) za preučevanje živega srebra v okolju. Radioaktivno sevanje 197Hg lahko namreč izredno natančno izmerimo, 197Hg pa se vede kemijsko enako kot drugi izotopi živega srebra. Značilnosti tega izotopa omogočajo raznovrstne študije kemijskih pretvorb in razvoj analiznih metod za merjenje koncentracij živega srebra v okolju. Med drugim smo na odseku z uporabo izotopa 197Hg odkrili omejitve trenutnih metod in razvili nove pristope za merjenje živega srebra v zraku, 197Hg pa smo uporabili tudi za raziskave živega srebra v vodi in sedimentih.
Pri teh raziskavah smo (po že opisanem postopku) 197Hg najprej proizvedli v jedrskem reaktorju, nato pa smo ga uporabili za kontrolirane laboratorijske eksperimente. Rezultate eksperimentov smo dobili z meritvami radioaktivnosti izotopa 197Hg, ki je pretežno sevalec gama. Za meritve smo uporabili detektorje, ki sevanje gama zaznajo preko germanijevega kristala in ga pretvorijo v računalniški signal. V eni od študij smo pogoje laboratorijskih eksperimentov približali tistim, ki jih najdemo v morju in oceanih, da bi tako izvedeli, ali se živo srebro v morski vodi lahko pretvori v druge oblike. Rezultati so pokazali, da se lahko anorgansko živo srebro (Hg2+) v morski vodi v manjši meri pretvori v bolj toksične organske oblike živega srebra in v elementarno živo srebro (Hg0). Izotop 197Hg je v tem primeru zaradi svoje visoke občutljivosti za meritve radioaktivnosti omogočil izvajanje eksperimentov pri izredno nizkih koncentracijah živega srebra, primerljivih s koncentracijami živega srebra v morski vodi. V sorodni študiji vedenja živega srebra v morski vodi smo z uporabo 197Hg ugotovili, da je kombinacija bakterij in svetlobe v vodi Tržaškega zaliva odgovorna za pretvorbo anorganskega živega srebra v elementarno. Na drugi strani smo 197Hg uporabili tudi za razvoj analiznih metod, saj lahko zaradi karakteristične radioaktivnosti tega izotopa živo srebro lažje spremljamo skozi celotni analizni postopek, s tem pa odkrijemo njegove omejitve in vpeljemo potencialne izboljšave. Na ta način smo v eni od raziskav razvili kalibracijsko metodo za oksidirane oblike živega srebra v zraku; pri tej metodi smo oksidirane oblike živega srebra proizvedli s pomočjo oksidacije elementarnega živega srebra v hladni plazmi. Hladna plazma (plazma, kjer se energija ne sprosti kot toplota, temveč v obliki visokoenergetskih elektronov) v kombinaciji z reaktivnimi plini kisikom (O2), klorom (Cl2) in bromom (Br2) je služila kot katalizator pretvorbe elementarnega živega srebra v živosrebrov oksid (HgO), živosrebrov klorid (HgCl2) in živosrebrov bromid (HgBr2). Kalibracijska metoda predstavlja pomemben prispevek k izboljšavi meritev živega srebra v zraku, ki so zaradi nizkih koncentracij različnih spojin živega srebra in njihove kemijske reaktivnosti zelo zahtevne za izvajanje.

Naslovnica revije Analytical Chemistry: prikaz kalibracijske metode za oksidirane oblike živega srebra v zraku, pri kateri smo za razvoj in optimizacijo metode uporabili 197Hg (povzeto po Gačnik idr. 2022)
S temi raziskavami pridobivamo pomembne informacije o tem, kako smo ljudje z emisijami živega srebra vplivali na njegovo količino v okolju okoli nas. Živo srebro je zdravju škodljiv nevrotoksin, določene spojine živega srebra se vse življenje akumulirajo v človeškem telesu, zato imajo lahko že relativno majhne spremembe v koncentraciji velik zdravstveni vpliv na populacijo. Najbolj znan zgodovinski primer, ki kaže, kako lahko majhne spremembe v količini živega srebra privedejo do velikega vpliva na ljudi, je minamatska katastrofa v petdesetih letih 20. stoletja. V japonskem zalivu Minamata se je vse začelo z mačkami, ki so začele kazati simptome tresavice, zmedenosti in težav z orientacijo. Simptomi so bili tako močni, da so mačke »poplesavale«, lokalni prebivalci pa so simptome poimenovali »vročica plešočih mačk«. Podobni nevrološki simptomi so se sčasoma pojavili tudi med ljudmi, dogajali so se tudi smrtni primeri. Raziskovalci so bolezen hitro povezali s pretežno morsko dieto ljudi (in mačk), nato pa še z živim srebrom, ki je v zaliv prihajalo iz tovarne kemikalij Chisso Corporation. Ker je tovarna delovala že od leta 1908, so odgovorni trdili, da obrat ne more biti vzrok onesnaženja, kasneje pa so odkrili, da je tovarna v tistem času zaradi spremembe katalizatorja določene kemijske reakcije začela proizvajati večji delež bolj toksične oblike živega srebra kot prej, in sicer metil živo srebro (MeHg+). Ta izredno nevrotoksična oblika živega srebra je v telesa ljudi prišla preko rib, ki so plavale v kontaminirani vodi zaliva. Torej je relativno majhna sprememba postopka proizvodnje prispevala k zastrupitvi mnogih ljudi, kar nakazuje na pomembnost razumevanja kemije živega srebra v okolju.

Raziskovalni jedrski reaktor TRIGA med obratovanjem, Institut "Jožef Stefan" (foto: Radojko Jaćimović)
Če povzamemo začetno primerjavo iz uvoda: zlato v našem primeru in v nasprotju s prizadevanji alkimije ni osrednji akter niti željeni produkt. Pa vendar – ali bi lahko z opisanim postopkom pretvorbe živega srebra v zlato obogateli? Ob hipotetičnem 12-urnem obsevanju nekaj mililitrov živosrebrne raztopine v sredici jedrskega reaktorja pridobimo krepko manj kot mikrogram (10−6 grama) zlata, torej je odgovor na dlani – ne, ne moremo postati bogati (o ceni materiala, obsevanja in delovne sile na tem mestu niti ne bomo razpravljali). Ker smo z živim srebrom v vsakodnevnem stiku, pa ima znanje, ki ga pridobimo pri izkoriščanju 197Hg za preučevanje vedenja živega srebra v okolju, izreden pomen za širšo družbo.















